Определите относительную влажность воздуха φ(%) при температуре 33°С, если точка росы равна 11°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 1,33 кПа и 5,02 кПа.
29
40
34
26
Также изучают: Колебания и волны, Гидростатика и гидродинамика, Ядерная физика, Итоговый тест (11 класс), географическое положение России (8 класс)
Определите относительную влажность воздуха φ(%) при температуре 33°С, если точка росы равна 11°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 1,33 кПа и 5,02 кПа.
29
40
34
26
Определите относительную влажность воздуха 9 (%) при температуре 31°С, если точка росы равна 11°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 1,33 кПа и 4,45 кПа.
24
36
49
32
Определите относительную влажность воздуха φ(%) при температуре 30°С, если точка росы равна 11°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 1,33 кПа и 4,19 кПа.
49
40
34
30
Определите относительную влажность воздуха φ(%) при температуре 29°С, если точка росы равна 11°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 1,33 кПа и 3,95 кПа.
36
49
30
32
Определите относительную влажность воздуха φ(%) при температуре 35°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 5,64 кПа.
24
28
32
18
Определите относительную влажность воздуха φ(%) при температуре 23°С, если точка росы равна 9°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 1,14 кПа и 2,78 кПа.
48
61
43
55,5
Определите относительную влажность воздуха φ(%) при температуре 30°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 4,19 кПа.
42
31
34
24
Определите относительную влажность воздуха φ(%) при температуре 31°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 4,45 кПа.
32
41
29
23
Определите относительную влажность воздуха φ(%) при температуре 32°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 4,73 кПа.
20
26
22
16
Определите относительную влажность воздуха φ(%) при температуре 34°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 5,32 кПа.
20
24
32
16
Определите относительную влажность воздуха φ(%) при температуре 20°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 2,33 кПа.
42
37
46
30
Определите относительную влажность воздуха φ(%) при температуре 21°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 2,46 кПа.
35
40
30
46
Определите относительную влажность воздуха φ(%) при температуре 22°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 2,62 кПа.
46
30
37
42
Определите относительную влажность воздуха φ(%) при температуре 33°С, если точка росы равна 6°С. Давления насыщенных паров при точке росы и данной температуре соответственно равны 0,93 кПа и 5,02 кПа.
26
21
32
16
В каких единицах измеряется коэффициент поверхностного натяжения: 1) Н/м; 2) Н/м2; 3) Дж/м; 4) Дж/м2; 5) Вт/м2?
2 и 3
1 и 4
1 и 5
только 5
Стеклянный капилляр длиной 1 м диаметром 1 мм, открытый с обоих концов, заполнен водой и находится в состоянии свободного падения в вертикальном положении. Какова высота столба воды, оставшейся в капилляре (см)?
1
10
50
100
Определите коэффициент поверхностного натяжения жидкости (мН/м) плотностью 0,8 г/см3, если она поднимается по капилляру диаметром 2 мм на высоту 7,5 мм.
73
24
40
30
Может ли ртуть вытекать из тонкого стеклянного капилляра каплями и почему?
нет, так как ртуть не смачивает стекло, она вытечет струей
нет, так как ртуть смачивает стекло
да, так как ртуть не смачивает стекло
да, так как ртуть смачивает стекло
Вода налита в цилиндрический сосуд радиусом 10 см. Определите поверхностную энергию воды (мкДж), если ее коэффициент поверхностного натяжения равен 73 мН/м.
2292
20,6
2,1
206
На какую высоту (см) поднимается вода (у=73 мН/м) в смачиваемом капилляре диаметром 0,73 мм, один конец которого опущен в воду.
8
6
4
2
Укажите правильную зависимость жёсткости стержня (k) от его длины (I), площади поперечного сечения (S) и модуля упругости (Е) материала стержня.
Е = IS/k
k = EI/S
Е = kS/I
k = ES/I
Как изменится масса капли воды, вытекающей из пипетки с диаметром отверстия 2 мм, по сравнению, с состоянием покоя, если пипетка будет двигаться вниз с ускорением 5 м/с2?
увеличится в 5 раз
увеличится в 4 раза
не изменится
увеличится в 2 раза
Стеклянная капиллярная трубка диаметром 1 мм, открытая с обоих концов, заполнена водой (у=73 мН/м) и закреплена на штативе вертикально. Какой высоты столб воды останется в трубке (см)?
2,9
292
29,2
5,8
При подвешивании груза проволока удлинилась на 9 мм. На сколько мм удлинится такая же проволока вдвое большей длины под тем же грузом?
4,5
36
18
9
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 70% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 67 °С.
10
3,4
4,5
7,5
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 60% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 67 °С.
4,5
10
7,5
3,4
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 80% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 57 °С.
4
7
9,96
5,3
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 70% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 57 °С.
4
5,3
7
9,9
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 500 м/с, пробив деревянный брусок, вылетает из него со скоростью 200 м/с. Какая часть пули (г) расплавилась, если ей передано 60% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 37 °С.
9,9
7,4
5,3
4
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 500 м/с, пробив деревянный брусок, вылетает из него со скоростью 200 м/с. Какая часть пули (г) расплавилась, если ей передано 70% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 37 °С.
5,8
10
7,3
2,4
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 500 м/с, пробив деревянный брусок, вылетает из него со скоростью 200 м/с. Какая часть пули (г) расплавилась, если ей передано 80% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули – 37 °С.
5,3
10
2,4
8,7
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 500 м/с, пробив деревянный брусок, вылетает из него со скоростью 200 м/с. Какая часть пули (г) расплавилась, если ей передано 50% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 47 °С.
6,4
10
8,7
5,8
Необходимо нагреть 3 кг льда от 0°С до 40°С. Удельная теплота плавления льда 330 кДж/кг, удельная теплоемкость воды 4200 Дж/кг•К. Какое количество теплоты (кДж) для этого требуется?
996
952
978
1494
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 60% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 57 °С.
9,9
4
7
5,3
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 60% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 47 °С.
7,5
10
3,4
4,5
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 500 м/с, пробив деревянный брусок, вылетает из него со скоростью 200 м/с. Какая часть пули (г) расплавилась, если ей передано 70% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 47 °С.
7,8
6,4
9,8
3
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 70% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 47 °С.
8,9
2,9
9,4
6,4
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 80% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 47 °С.
9,4
7,9
6,4
2,9
Температура нагревателя реальной тепловой машины равна 427°С, температура холодильника 127° С. Тепловая машина за один цикл получает от нагревателя тепловую энергию 600 Дж и отдает холодильнику 400 Дж. Какую часть от КПД идеальной машины составляет КПД данной реальной машины?
7/9
6/7
1/2
7/8
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 60% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 37 °С.
2,9
8,9
9,4
6,4
Количество теплоты, которое нужно передать трем молям идеального одноатомного газа, чтобы увеличить при постоянном давлении его температуру Т0 в 2 раза, равно (R – универсальная газовая постоянная):
5RT0
15RT0 / 2
3RT0 /2
2RT0
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 80% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 37 °С.
6,4
5,4
2,9
8,9
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 70% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 37 °С.
8,4
5,9
2,4
4,4
Газ расширяется от объема V1 до V2:
1) изобарно;
2) изотермически;
3) адиабатно.
В каком случае совершаемая работа будет наибольшей?
3
1
2
1 и 2
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 60% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 27 °С.
6,9
2,4
5,4
8,4
Свинцовая пуля массой 10 г, летевшая горизонтально со скоростью 400 м/с, пробив деревянный брусок, вылетает из него со скоростью 100 м/с. Какая часть пули (г) расплавилась, если ей передано 80% энергии, выделившейся в процессе пробивания бруска? У свинца удельная теплоемкость 130 Дж/кг•К, удельная теплота плавления 25 кДж/кг, температура плавления 327°С, а начальная температура пули - 67 °С.
10
3,4
7,5
4,5
На сколько джоулей увеличится внутренняя энергия одноатомного идеального газа, находящегося в цилиндрическом сосуде со свободным поршнем, при сообщении газу количества теплоты 500 Дж?
100
180
250
300
Сколько килограммов солярки затрачивает за 3 часа дизельный двигатель мощностью 42 кВт, если КПД его равен 20%? Удельная теплота сгорания солярки 42 МДж/кг
54
36
21
28
Во сколько раз температура нагревателя (К), должна быть выше температуры холодильника идеальной тепловой машины, чтобы ее КПД был 50%?
5
4
3
2
Температура нагревателя идеальной тепловой машины 600К, холодильника - 300К и за один цикл рабочее тело получает от нагревателя 2400 Дж энергии. Определите работу, совершаемую газом за один цикл.
300
1500
1200
3000
Также изучают: Колебания и волны, Гидростатика и гидродинамика, Ядерная физика, Итоговый тест (11 класс), географическое положение России (8 класс)
Задумывались ли вы когда-нибудь о том, как устроена наша Вселенная? Почему все происходит именно так, как оно происходит? Почему мы живем именно на Земле, а не на Марсе? Как вообще появились звезды на небе? На все эти вопросы может ответить (ну или постараться ответить) одна из самых интересных наук – Астрономия.

Не путайте науку о Вселенной с псевдонаукой о гороскопах Астрологией. Да, их темы соприкасаются со звездами и планетами и в самом начале они шли бок о бок друг с другом, однако, принципы астрологии не подтверждаются научными методами. Да и астрология в основном про черты характера и судьбы людей, а не про то, как устроен космос. Я соглашусь, эта лженаука может быть интересной и информативной для кого-то, но поверьте мне, астрономия куда круче.
И так, что же за наука эта астрономия и с чем ее едят? Начнем, пожалуй, с простого – с определения.
Астрономия (от греческого – звезда и закон) – это наука о Вселенной, которая изучает небесные тела (то есть звезды, планеты, галактики, астероиды и так далее), а также их движение, структуру, происхождение и развитие. Но на этом астрономия не заканчивается! Наука о звездах охватывает множество разделов, таких как небесная механика (движение тел), астрофизику (физику тел), космологию (Вселенную в целом) и планетологию (планеты и спутники).
Астрономия это одна из древнейших естественных наук, которая берет свое начало еще до нашей эры. Представьте себе, Вы живете во II веке до нашей эры, в мире еще нет такого понятия как «световое загрязнение». Ночи невероятно темные, а на ночном небе видно 2-3 тысячи мерцающих точек и все это выглядит невероятно красиво. Вы ориентируетесь на фазы луны, чтобы определить какой на дворе день и месяц. Благодаря чистейшему небу, Вы определяете стороны света для навигации и времени. Звучит здорово, не так ли?
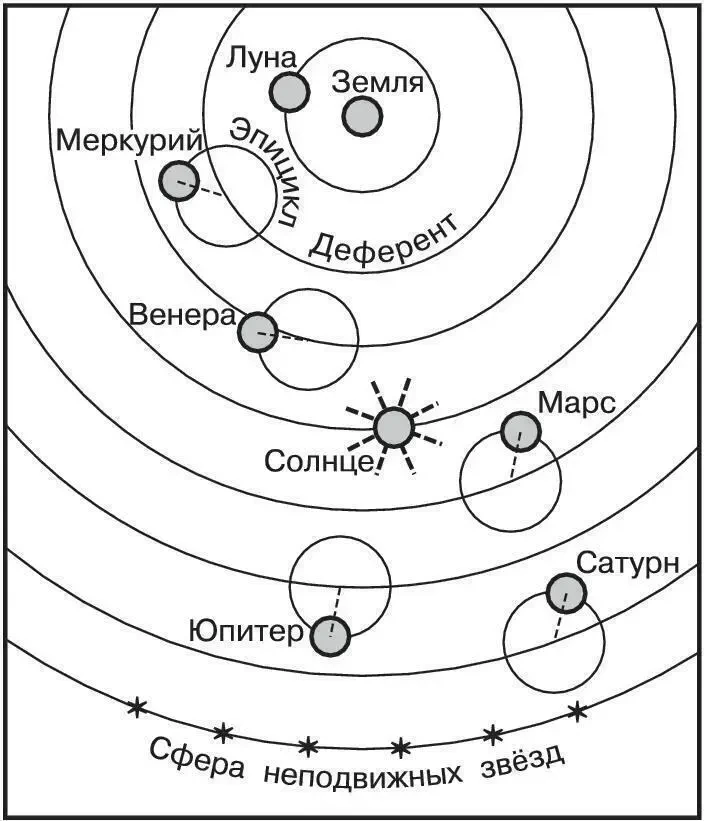
VI век. Древнегреческий философ Аристотель думал также. Ученик Платона свел все сведения того времени о небесных явлениях и движениях светил в стройную теорию. Аристотель, основываясь на теорию движения планет Евдокса Книдского IV века до нашей эры, приписал планетным сферам реальное физическое существование.
Но что за теория движения планет? Книдский объяснял эту теорию как видимое движение планет комбинацией равномерных круговых движений, вращающихся вокруг Земли. Для каждой планеты (и Солнца, и Луны) Евдокс использовал несколько сфер (от 3 до 4), полюса которых были закреплены на предыдущей сфере, создавая сложные траектории для объяснения попятного (ретроградного) движения.
«Стоп, что? Попятное движение? Ретроградное движение? Это как-то относится к тому, что у меня болит голова во время ретроградного меркурия?»
Нет!
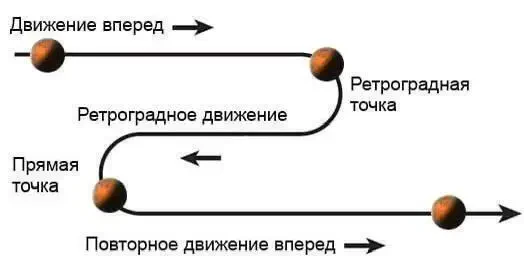
Ретроградное или попятное движение – это кажущееся движение небесного тела (например, планеты) в направлении, противоположном его обычному движению на фоне звезд.
«Ничего не понятно…А можно простыми словами?...»
Итак, как же это выглядит. Планеты просто движутся по небу, а Земля, двигаясь быстрее, «обгоняет» медленную внешнюю планету. Из-за того, что Земля обогнала планету, кажется, что она остановилась, и как только Земля проходит дальше этой планеты, то она снова начинает двигаться вперед.
Это было только начало астрономии.
Вернемся обратно к теории. В сумме эти сферы насчитывали 27 сфер для всех светил, включая неподвижных звезд. И что же эта теория дает, спросите Вы. А она успешно объясняла движения наблюдаемых планет. Вы наверняка заметили, как Книдский и Аристотель считают, что в центре Вселенной находилась неподвижная Земля, которая еще и не вращается вокруг своей оси. Но мы все знаем, что это не так. Как же тогда люди пришли к такому выводу?
«Гелиоценрическая модель мира – представление о том, что Солнце является центральным небесным телом, вокруг которого вращаются Земля и другие планеты»

Ответ на вопрос, как люди пришли к данной модели очень прост. А все благодаря наблюдениям и математическим расчетам, которые показали, что модель «Земли в центре» сложна и плохо объясняет движение планет.
Да, вот она наука. Все ответы мы находим через наблюдения и расчеты.
Но кто же человек, стоящий за таким великим открытием? Это был Николай Коперник – польский и немецкий астроном и математик эпохи Возрождения. Как он пришел к выводу о гелиоцентрической модели мира? Правильно – благодаря наблюдениям и подсчетам, мы же, все таки, о науке говорим))
Вообще, Коперник, как и другие, видел сложности в модели, где Земля была в центре и не вращалась. Поэтому, он заметил, что поместив Солнце в центр и сделав Землю одной из вращающихся планет, это объясняло движения планет в более естественном ключе.
Стоит также отметить, что именно Коперник постулировал, что Земля совершает три движения:
Деклинационное движение – это годичное движение оси Земли, которое происходит параллельно самой себе и приводит к видимому годичному движению Солнца. То есть, когда Солцне меняет свою высоту над горизонтом в течении года, то поднимаясь выше летом, то опускаясь ниже зимой. При этом, оно не меняет своего положения, а просто «танцует» вверх-вниз на небесной сфере.
Может быть, Вы видели видео в интернете, как автор мог снимать как движется Солнце в течении года, оставляя камеру на одном месте. Это на самом деле, выглядит очень интересно, и наглядно показывает, как «танцует» Солнце в деклинационном движении.

Но почему вообще Солнце в центре нашей системы? Почему именно звезда, а не какая-нибудь планета? Солнце находится в центре Солнечной системы, потому что оно является самым массивным объектом. А содержание 99,866% всей массы системы и мощная гравитация удерживает все планеты, астероиды и кометы на орбитах вокруг себя. А как появилось Солнце? Все началось с облака газа и пыли, из которого уже сформировалось Солнце, а вокруг него из остатков вещества образовался диск, из которого возникли планеты.
Солнце – это звезда, потому что массивное самосветящееся небесное тело, состоящее из горячей плазмы (водород и гелий), в ядре которого происходят термоядерные реакции, выделяющие свет и тепло, вокруг которого вращаются планеты.
Вы наверняка видели в новостных канал или просто в интернете, про вспышки Солнца, что некоторые могут быть очень большими и влиять на физическое состояние людей.
Знали ли Вы, что данные вспышки происходят из-за внезапного высвобождения накоплений магнитной энергии в атмосфере Солнца. Часто в областях, солнечных пятен, где магнитные поля становятся чрезвычайно сложными, переплетаются и разрываются, что приводит к взрывному выделению огромного количества энергии в виде света, тепла и заряженных частиц.

Но такие солнечные вспышки, на самом деле опасны. Если бы у Земли не было мощного магнитного поля, которое отклоняет заряженные частицы и плотная атмосфера, которая поглощает вредное излучение, то наша планета выглядела бы как Марс, который потерял свое глобальное магнитное поле еще в далеком прошлом.

Интересный факт: Вы можете увидеть невооруженным глазом солнечные вспышки, и это называется северное сияние! Это происходит из-за того, что солнечные вспышки проходят в верхних слоях атмосферы Земли, когда заряженные частицы солнечного ветра, направляемые магнитным полем планеты к полюсам, сталкиваются с молекулами газов и заставляют их светиться разными цветами.

Признаться честно, в сфере астрономии просто невероятно много информации, которую можно обсуждать часами. Как устроена Вселенная, почему именно так, как все зародилось и что будет после. То, что Вы прочли в этой статье это самая-самая верхушка айсберга. Потому что можно бесконечно обсуждать космос, звезды, астероиды, планеты. Ведь в этой неимоверно огромной и бесконечной Вселенной столько же много загадок, теорий и ответов.
А я, безумно надеюсь, что когда-нибудь люди узнают все тайны космоса, хотя возможно это далеко за гранью человеческого понимания. И надеюсь, что эта статья задала Вам начало любви к астрономии, ну или просто Вы удовлетворили свою потребность в прочтении чего-то космического)
Представьте себе утро, когда вы просыпаетесь, а ваш смартфон не просто будит вас, а предсказывает весь день: идеальный маршрут без пробок, лекарство от простуды, сгенерированное под ваш геном, и инвестиции, которые вырастут в реальном времени. Эта вычислительная мощь — не из кремния, а из самой природы частиц, перенесённой в машины.
Квантовые компьютеры обещают именно такую картину: сверхбыструю, умную силу, способную перевернуть нашу цифровую жизнь. Но вот парадокс — с 1980-х годов, когда первые учёные зажгли искру идей, мы потратили сотни миллиардов долларов, а ваш ноутбук по-прежнему мучается с простыми задачами.
Почему так происходит? Что мешает этой 'квантовой' революции хлынуть в наши гаджеты? И главное — сколько ещё ждать, пока она станет реальностью? Давайте нырнём в эту историю глубже, шаг за шагом разбирая факты, достижения и препоны. Я опираюсь на свежие отчёты из надежных источников — от McKinsey и MIT до ассоциаций квантовых компаний, — чтобы всё было по-честному, без домыслов.
Квантовый компьютер — это не магия, а чистая физика, которая уже миллиарды лет работает в атомах. Представьте два крошечных шарика — биты в обычном ПК, которые могут быть только 0 или 1. Они отталкиваются от сложностей, как магниты, но если применить квантовые эффекты — суперпозицию и запутанность, — они сближаются с такой силой, что решают задачи параллельно. В этот миг высвобождается огромный заряд вычислений: из частиц рождается мощь, которая может оптимизировать весь интернет.
Почему это кажется идеальным? Потому что кванты решают сразу несколько глобальных головоломок. Вот ключевые плюсы, подтверждённые расчётами экспертов из MIT и McKinsey:
Эти преимущества уже привлекают внимание бизнеса и науки, открывая двери для инноваций, о которых раньше можно было только мечтать. Но, конечно, не всё так просто — технология требует идеальных условий, и именно это делает её такой сложной в реализации.
Но вот в чём соль: в лаборатории кубиты держатся миг из-за шума, как сигнал в помехах. Чтобы они работали стабильно, как в природе, нужно преодолеть барьеры, которые держат нас в напряжении десятилетиями. А пока давайте вспомним, как всё начиналось — эта история полна драмы, триумфов и неожиданных поворотов.
Всё пошло в 1980-е, когда человечество, ещё не отошедшее от первых ПК, начало мечтать о сверхвычислениях. В 1981 году в лаборатории физик Ричард Фейнман предложил идею: использовать квантовые эффекты, чтобы моделировать природу. Это был прорыв, но первые эксперименты обернулись разочарованием.
Вспомним первые алгоритмы — в 1994 году Питер Шор придумал способ взлома шифров. Учёные объявили о сенсации, но через годы выяснилось: это всего лишь теория. Такой урок научил: кванты требуют терпения. В 1990-х в США изобрели первые кубиты — устройства, где частицы "крутятся" в суперпозиции, не давая ошибкам коснуться расчётов. Это стало стандартом: сегодня 90% экспериментов используют такие подходы.
2000-е принесли надежду. В лабораториях, как у IBM, стабилизировали кубиты для первых цепочек — на пороге реакции. Но мощности выходило меньше, чем вкладывали. 2010-е — эра облачных квантов: в Google калибровали системы, чтобы сжимать задачи в миг. А в 2019 году на Sycamore в США кубиты продержались микросекунды при полной мощности. Учёные ликовали: это был первый шаг к 'преимуществу' — моменту, когда квант обходит классику.
2020-е объединили мир. Стартовали проекты вроде Quantum Flagship в ЕС. 35 стран, включая США, ЕС, Китай, вложили миллиарды. Цель: доказать, что кванты работают на масштабе. Строительство шло, но задержки из-за цепочек поставок сдвинули график. К 2025 году проект вышел на новый уровень: в октябре установили новые чипы, а системы вроде Willow завершены. Первый реальный расчёт запланирован на конец года, а полноценные операции — на 2030-е. Несмотря на риски, это даёт надежду. Такие шаги показывают, как из чистой теории технология превращается в реальные машины, способные менять мир.
Сегодня кванты — не только государственная монополия. Более 70 частных компаний по миру строят компактные версии, а общее число установок превысило 160. Это как если бы в 1980-х вместо одной лаборатории расцвёл целый лес стартапов — и всё благодаря деньгам, которые хлынули рекой.
Если кванты — это марафон, то инвестиции — топливо для бегунов. С 1980-х мир вбухал в них сотни миллиардов: только государственные программы США, Европы и Азии — около 100 миллиардов долларов. Но настоящий взрыв случился недавно. По отчётам McKinsey на конец 2025 года, частные инвестиции превысили 2 миллиарда долларов глобально — рост в пять раз с 2020-го. За последние месяцы компании привлекли миллиарды — рекорд, который бьёт все предыдущие.
Кто стоит за этим? Не только энтузиасты в белых халатах, а тяжеловесы бизнеса и политики. Разберём по полочкам:
Эти деньги не просто лежат: компании наняли тысячи специалистов, плюс цепочки поставок — рост в четыре раза за пять лет. Но 83% фирм жалуются: нужно ещё миллиарды на пилоты. Это как строить космический корабль — каждый болт стоит fortune, но без него не взлетишь. Такие вложения уже дают плоды: от новых чипов до первых коммерческих контрактов, ускоряя переход от лабораторий к реальному бизнесу.
И вот вопрос: а окупается ли? По моделям, кванты добавят триллионы к глобальному ВВП к 2050-му, сделав вычисления дешевле на 50%.
Теперь к горькой правде: несмотря на бабло и мозги, кванты упорно не выходят на рынок. Это не лень или заговор — а суровая физика и инженерия. Представьте, что вы пытаетесь удержать в руках горсть песка во время урагана: вот так и кубиты — капризные, неуловимые. Вот топ-барьеры, подтверждённые отчётами DOE и McKinsey на 2025 год:
Эти проблемы — не стена, а лестница. Каждый шаг, как в новых чипах, приближает вершину, но спотыкания бывают. И всё же прогресс ускоряется: от снижения ошибок до новых материалов, которые делают кванты ближе к реальности.
Текущий прогресс – от лабораторных вспышек к заводам будущего.
Хорошие новости перевешивают: 2025-й — год, когда кванты вышли из тени. McKinsey выделяет шесть трендов: рост инвестиций, ИИ в моделировании, компактные дизайны, партнёрства с гигантами, глобальные цепочки и фокус на материалах. Более 160 установок по миру тестируют идеи — от ионных ловушек до фотонных.
Государственные флагманы в действии:
Эти проекты уже показывают реальные преимущества, от симуляций молекул до оптимизации, доказывая, что переход к коммерции не за горами.
Частники — мотор прогресса, фокусируясь на скорости и миниатюре. Вот лидеры по отчётам The Quantum Insider:
Другие — Xanadu с фотонными чипами, Quantinuum с ионными. 84% компаний верят в сеть к 2030-м, половина — к 2035-му. Это не фантазия: в 2025-м фирмы дебютировали машинами, достигшими 'quantum-friendly' скоростей. Такие инновации уже привлекают клиентов из бизнеса, показывая, как квант выходит за пределы лабораторий.
Кванты не заменят ваш ПК, но перевернут IT. По отчётам PwC и BCG, влияние на крипто, AI, облака:
Эти изменения уже начинаются: от гибридных систем до новых стандартов безопасности, заставляя IT-лидеров готовиться заранее.
Опросы McKinsey дают картину: первые пилоты — начало 2030-х, полная коммерция — середина десятилетия. DOE ставит mid-2030s как цель, с фокусом на этапы: демонстрации (3–5 лет), пилоты (5–10 лет) и флот (10+ лет). Но риски: задержки могут сдвинуть на 2040-е.
Что ускорит? Вот возможные катализаторы:
Если всё сложится, кванты покроют 10% вычислений к 2050-му, по моделям. Но даже если нет — каждый тест учит. Такие прогнозы основаны на реальном прогрессе, от снижения ошибок до первых доходов компаний.
Квантовые компьютеры — это сага о человеческом упорстве: от разочарований Фейнмана к рекордам Willow, от миллиардов в проектах к заводам IonQ. Миллиарды не зря — они строят мост к миру, где вычисления дешёвые, как воздух, и умные, как природа. Прорыв в 2030-х изменит всё: от AI без границ до сетей без взломов. Пока ждём, давайте ценить шаги — они освещают путь. А вы? Готовы ли к утру, когда квант зажжётся в вашей сети? Это не 'если', а 'когда' — и оно ближе, чем кажется.
Стандартная модель — это фундаментальная теория, описывающая элементарные частицы и три из четырёх известных фундаментальных взаимодействий: электромагнитное, слабое и сильное. Она объединяет результаты десятилетий экспериментов и представляет собой краеугольный камень физики высоких энергий.
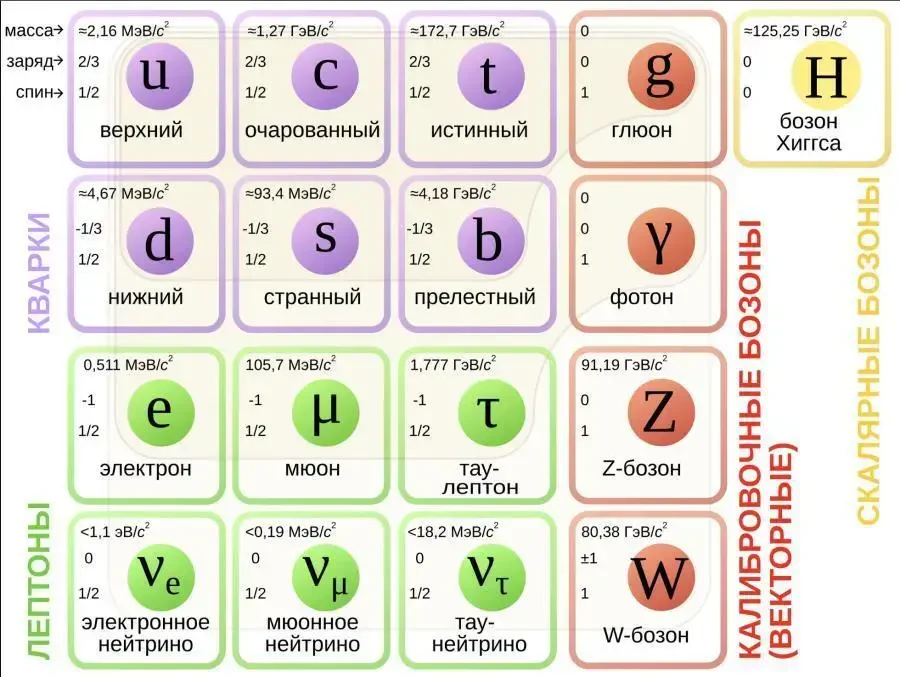
Стандартная модель включает:
1. Фермионы — частицы вещества:
2. Бозоны — переносчики взаимодействий:
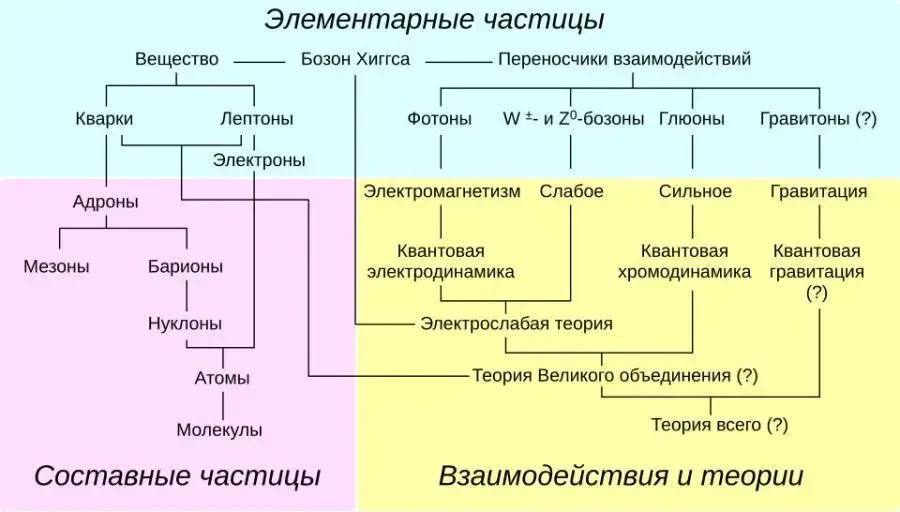
Стандартная модель предсказывала существование многих частиц, включая Хиггсовский бозон, который был обнаружен в 2012 году на Большом адронном коллайдере. Её предсказания с высокой точностью подтверждаются экспериментами.

Модель не объясняет:
Стандартная модель — мощная и проверенная теория, которая объясняет большинство наблюдаемых явлений в микромире. Однако её неполнота побуждает физиков искать «новую физику» за её пределами — в теориях, таких как суперсимметрия, теория струн и квантовая гравитация.
Звук — неотъемлемая часть нашей повседневной жизни. Мы слышим голоса, музыку, шум дождя — но что именно стоит за этими звуками с точки зрения физики?

С научной точки зрения, звук — это механическая волна, которая возникает в результате колебаний частиц упругой среды. Это значит, что звук не может распространяться в пустоте (вакууме) — ему нужна среда: воздух, вода или твёрдые тела.
Когда источник звука (например, струна гитары или голосовые связки человека) начинает колебаться, он создаёт сжатия и разрежения в окружающей среде. Эти колебания передаются от частицы к частице, образуя продольную волну.
Звуковая волна описывается несколькими физическими параметрами:
Человеческое ухо улавливает звуковые волны, которые попадают в ушной канал, вибрируют барабанную перепонку и передаются во внутреннее ухо. Там они преобразуются в электрические импульсы и передаются в мозг, где и происходит восприятие звука.
Человеческое ухо улавливает частоты в диапазоне от 20 Гц до 20 000 Гц. Звуки ниже 20 Гц называются инфразвуком, выше — ультразвуком.
На Луне звук не распространяется — ведь там нет атмосферы, а значит, и среды, способной передать звуковые колебания. Там можно лишь "услышать" вибрации через контакт с объектом, но не по воздуху.
Звук — это не просто ощущение, это физическое явление, в котором участвуют колебания, энергия и законы движения. Понимание физики звука важно для инженеров, музыкантов, врачей и всех, кто работает со звуком и технологиями.